Содержание
Производство серной кислоты | CHEMEGE.RU
Серную кислоту в промышленности производят из серы, сульфидов металлов, сероводорода и др. Один из вариантов — производство серной кислоты из пирита (серного колчедана) FeS2.
Основные стадии получения серной кислоты :
- Сжигание или обжиг серосодержащего сырья в кислороде с получением сернистого газа.
- Очистка полученного газа от примесей.
- Окисление сернистого газа в серный ангидрид.
- Взаимодействие серного ангидрида с водой.
Рассмотрим основные аппараты, используемые при производстве серной кислоты из пирита (контактный метод):
| Аппарат | Назначение и уравнения реакций |
| Печь для обжига | 4FeS2 + 11O2 → 2Fe2O3 + 8SO2 + Q Измельченный очищенный пирит сверху засыпают в печь для обжига в «кипящем слое«. |
| Циклон | Из печи выходит печной газ, который состоит из SO2, кислорода, паров воды и мельчайших частиц оксида железа. Такой печной газ очищают от примесей. Очистку печного газа проводят в два этапа. Первый этап — очистка газа в циклоне. При этом за счет центробежной силы твердые частички ссыпаются вниз. |
| Электрофильтр | Второй этап очистки газа проводится в электрофильтрах. При этом используется электростатическое притяжение, частицы огарка прилипают к наэлектризованным пластинам электрофильтра). |
| Сушильная башня | Осушку печного газа проводят в сушильной башне – снизу вверх поднимается печной газ, а сверху вниз льется концентрированная серная кислота.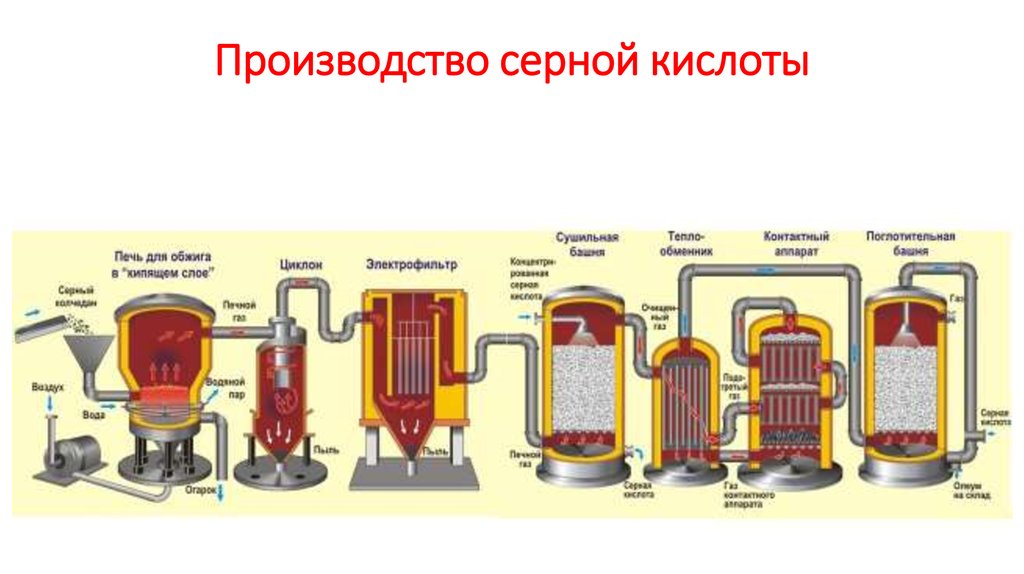 |
| Теплообменник | Очищенный обжиговый газ перед поступлением в контактный аппарат нагревают за счет теплоты газов, выходящих из контактного аппарата. |
| Контактный аппарат | 2SO2 + O2 ↔ 2SO3 + Q В контактном аппарате производится окисление сернистого газа до серного ангидрида. Процесс является обратимым. Поэтому необходимо выбрать оптимальные условия протекания прямой реакции (получения SO3):
Как только смесь оксида серы и кислорода достигнет слоев катализатора, начинается процесс окисления SO2 в SO3. Образовавшийся оксид серы SO3 выходит из контактного аппарата и через теплообменник попадает в поглотительную башню. |
| Поглотительная башня | Получение H2SO4 протекает в поглотительной башне. Однако, если для поглощения оксида серы использовать воду, то образуется серная кислота в виде тумана, состоящего из мельчайших капелек серной кислоты. Для того, чтобы не образовывался сернокислотный туман, используют 98%-ную концентрированную серную кислоту. Оксид серы очень хорошо растворяется в такой кислоте, образуя олеум: H2SO4·nSO3. nSO3 + H2SO4 → H2SO4·nSO3 Образовавшийся олеум сливают в металлические резервуары и отправляют на склад. |
Общие научные принципы химического производства:
- Непрерывность.
- Противоток
- Катализ
- Увеличение площади соприкосновения реагирующих веществ.
- Теплообмен
- Рациональное использование сырья
Понравилось это:
Нравится Загрузка…
Производство серной кислоты: SensoTech GmbH
Серная кислота (H2SO4) является одним из важнейших основных химических веществ. Стабильный спрос на нее растет, так как ее благоприятные свойства делают ее полезной при приготовлении разнообразных продуктов.
Существует несколько применений анализатора LiquiSonic® для измерения концентраций серной кислоты и олеумов:
- H2SO4 и добыча нефти
- производство удобрений
- сушка синтез-газа
- травление и маринованные ванны
- глубокая переработка руд
- катализ НПЗ
- производство различных химикатов
Два основных производственных процесса H2SO4 включают в себя, прежде всего, «двухконтактную двойную абсорбцию» (DCDA) — процесс с использованием катализатора на основе пенооксида ванадия (V2O5) для получения высококонцентрированного H2SO4 и олеума. Второе применение, разработанное в 1980 году, позволяет удалять серу из различных технологических газов с помощью метода, известного как «мокрая серная кислота» (WSA). Анализатор легко интегрируется в технологические стадии. Технология быстрого и надежного обнаружения LiquiSonic® улучшает использование активов, безопасность процесса и выход продукта.
Второе применение, разработанное в 1980 году, позволяет удалять серу из различных технологических газов с помощью метода, известного как «мокрая серная кислота» (WSA). Анализатор легко интегрируется в технологические стадии. Технология быстрого и надежного обнаружения LiquiSonic® улучшает использование активов, безопасность процесса и выход продукта.
Двойной контактный процесс двойного поглощения
DCDA использует различные исходные материалы, которые при различных реакциях синтезируются в диоксид серы. Первоначально SO2-содержащий газ поступает в сушильную башню для удаления содержащейся в нем воды. Затем газ сталкивается с тремя слоями катализатора в конвертере, где SO2 окисляется в SO3:
SO2 + 0.5 O2 → SO3
Затем SO3 поступает в промежуточную абсорбционную колонну (IAT). Хотя поглощение SO3 в водном растворе возможно, такая сильная экзотермическая реакция может привести к коррозии и разрушению установки.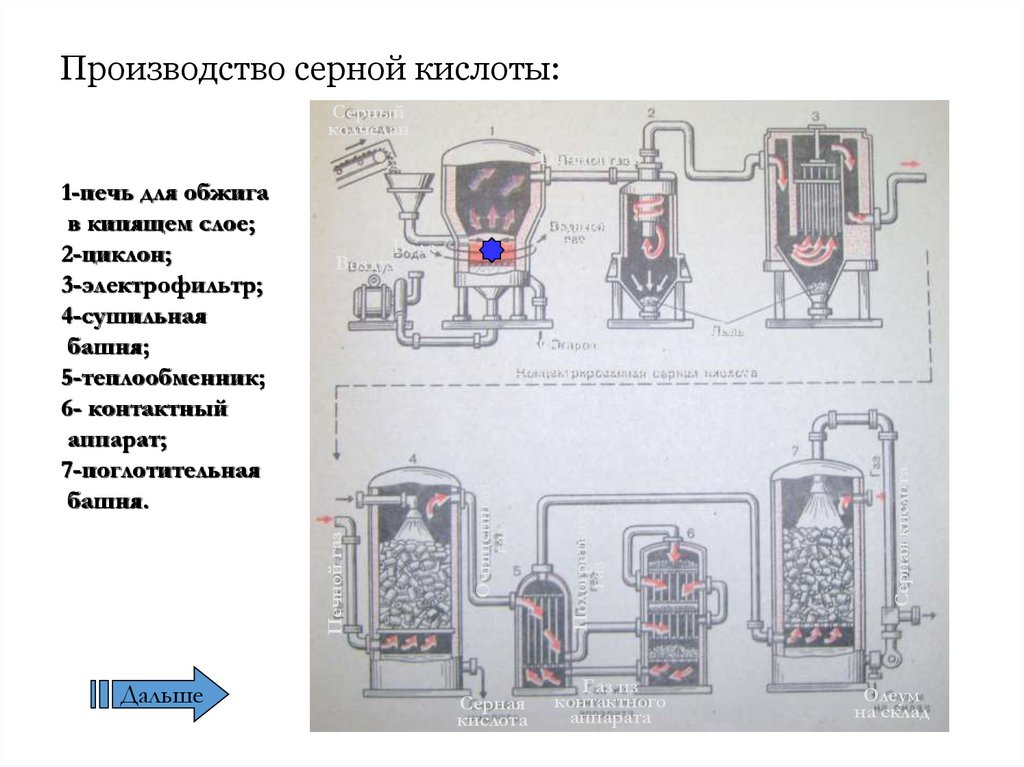 Вместо этого SO3 реагирует с содержанием воды 98 wt% H2SO4, образуя суперконцентрированный H2SO4:
Вместо этого SO3 реагирует с содержанием воды 98 wt% H2SO4, образуя суперконцентрированный H2SO4:
SO3 + H2O → H2SO4
Чтобы избежать загрязнения окружающей среды, SO2-содержащий отработанный воздух, выходящий из IAT, снова проходит через конвертер для подготовки SO3 к переработке в концентрированный h3SO4 в конечной абсорбционной башне (FAT). При переработке DCDA в качестве промежуточного продукта образуется олеум, состоящий из 100-ваттного% H2SO4, обогащенного SO3 — также известный как серная кислота или дисульфиновая кислота. Области применения включают в себя:
- производство высококонцентрированного H2SO4
- производство капролактама и нейлона
- процесс азотирования в сочетании с азотной кислотой
Нефть вырабатывается путем поглощения SO3 в башне, поглощающей олеум. Сенсоры LiquiSonic® обеспечивают превосходное управление процессом в диапазоне концентраций нефти 20 — 30 Вт и 50 — 60% Вт. Датчики LiquiSonic® могут быть установлены на подающих и обратных линиях абсорбционных башен и после блока разбавления.
Сенсоры LiquiSonic® обеспечивают превосходное управление процессом в диапазоне концентраций нефти 20 — 30 Вт и 50 — 60% Вт. Датчики LiquiSonic® могут быть установлены на подающих и обратных линиях абсорбционных башен и после блока разбавления.
Мокрый сернокислотный процесс
Первоначально процесс WSA был разработан для удаления сернистых компонентов из отходящих газов различных промышленных производственных процессов с широким спектром исходных материалов, которые могут приводить к образованию SO2. В отличие от DCDA, водяной пар остается в газе SO2. Благодаря специальному ванадиевому катализатору, пар не оказывает негативного влияния на каталитическое окисление из SO2 в SO3 в конвертере. Точки измерения LiquiSonic® в процессе WSA Наконец, газ SO3 поступает в конденсатор WSA, где водяной пар конденсируется для превращения SO3 в H2SO4. Концентрация продуктов H2SO4 составляет 98 Вт%. Измеряя концентрацию в линию, датчики LiquiSonic® устанавливаются на выходных линиях как для конденсатора WSA, так и для блока разбавления.
Измеряя концентрацию в линию, датчики LiquiSonic® устанавливаются на выходных линиях как для конденсатора WSA, так и для блока разбавления.
Клиентская ценность
Благодаря высокой чувствительности скорости звука к концентрации серной кислоты, датчики LiquiSonic® могут достигать непревзойденной точности ± 0,03 wt%. LiquiSonic® преодолевает двойную чувствительность, как по проводимости, так и по плотности, генерируя четкий сигнал в диапазоне концентраций 80-100 мас.% H2SO4, как показано на графике ниже, для получения надежных данных процесса в реальном времени. В случае деградации кислоты до уровня ниже 95 масляных%, LiquiSonic® обнаруживает, что критическая кислота «убегает», чтобы уменьшить вероятность повреждения теплообменника или других компонентов, повышая безопасность процесса и контроль.
Поточный анализатор LiquiSonic® позволяет сократить ручные лабораторные измерения, экономя трудовые и материальные затраты при титровании в типичном лабораторном бюджете для измерения серной кислоты:
- время отбора проб: 15 минут
- частота выборки: 6 раз в сутки
- окупаемость инвестиций в течение 13 месяцев
Дополнительные преимущества измерительных систем LiquiSonic® включают в себя:
- простая, удобная установка (plug&play)
- превосходная долгосрочная стабильность
- один датчик для всех применений (сниженные инвестиционные затраты)
- всесторонний диагностический потенциал
- соответствие всем необходимым диапазонам концентрации с высокой точностью
- улучшенный контроль процесса и безопасность
Sulfuric acid production with LiquiSonic
®
The LiquiSonic® analyzer can easily be integrated into different process stages. The rapid, robust sensing technology improves asset utilization, process safety and product yield.
The rapid, robust sensing technology improves asset utilization, process safety and product yield.
Sulfuric acid production with LiquiSonic®
Серная кислота
Серная кислота является одним из наиболее важных соединений, производимых в химической промышленности. Он используется для производства буквально сотен соединений, необходимых почти в каждой отрасли.
Использование серной кислоты
Наибольшее количество серной кислоты используется для производства фосфорной кислоты, которая, в свою очередь, используется для производства фосфатных удобрений, дигидрофосфата кальция и фосфатов аммония. Он также используется для производства сульфата аммония, который является особенно важным удобрением в условиях дефицита серы.
Рисунок 1 Использование серной кислоты.
Он широко используется в обработке металлов, например, при производстве меди и цинка, а также при очистке поверхности стального листа, известной как «протравка», перед покрытием тонким слоем олова, используемым для сделать банки для еды.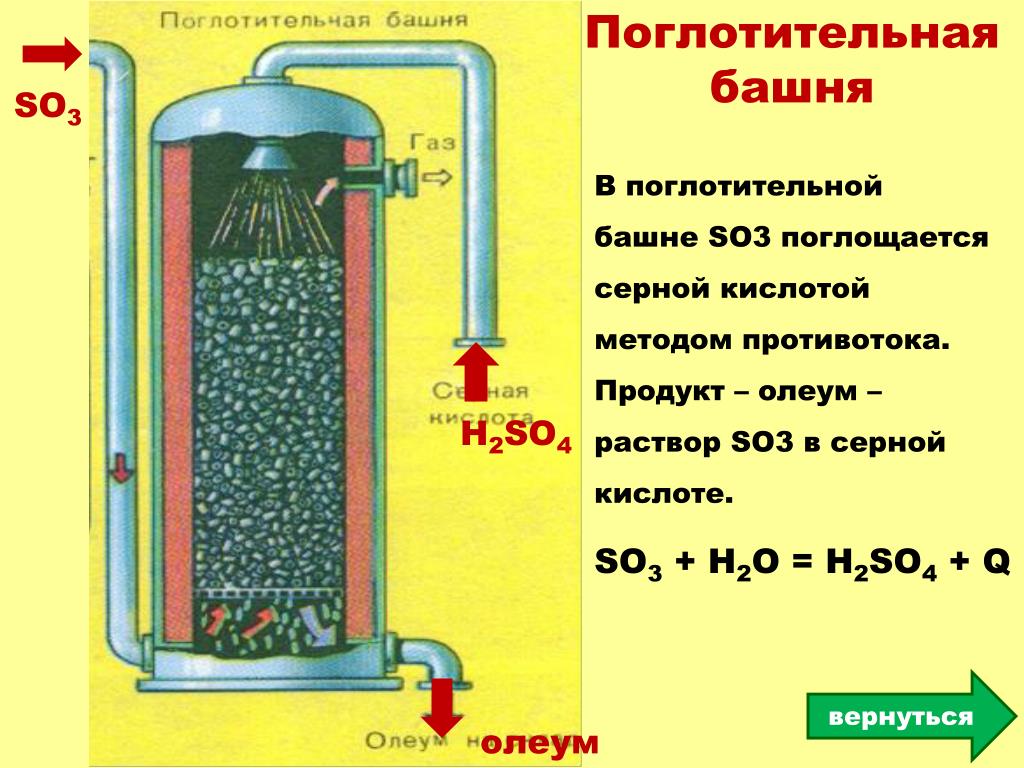
Применяется также для получения капролактама, перерабатываемого в полиамид 6, и в производстве диоксида титана, используемого, например, в качестве пигмента.
Среди многих других его применений — производство плавиковой кислоты и фенола с пропаноном, которые используются во многих отраслях промышленности.
Годовое производство серной кислоты
| Мир | 231 млн тонн |
| Китай | 74 миллиона тонн |
| США | 37 миллионов тонн |
| Индия | 16 миллионов тонн |
| Россия | 14 миллионов тонн |
| Марокко | 7 миллионов тонн |
Расчетные данные:
Merchant Research & Consulting Ltd.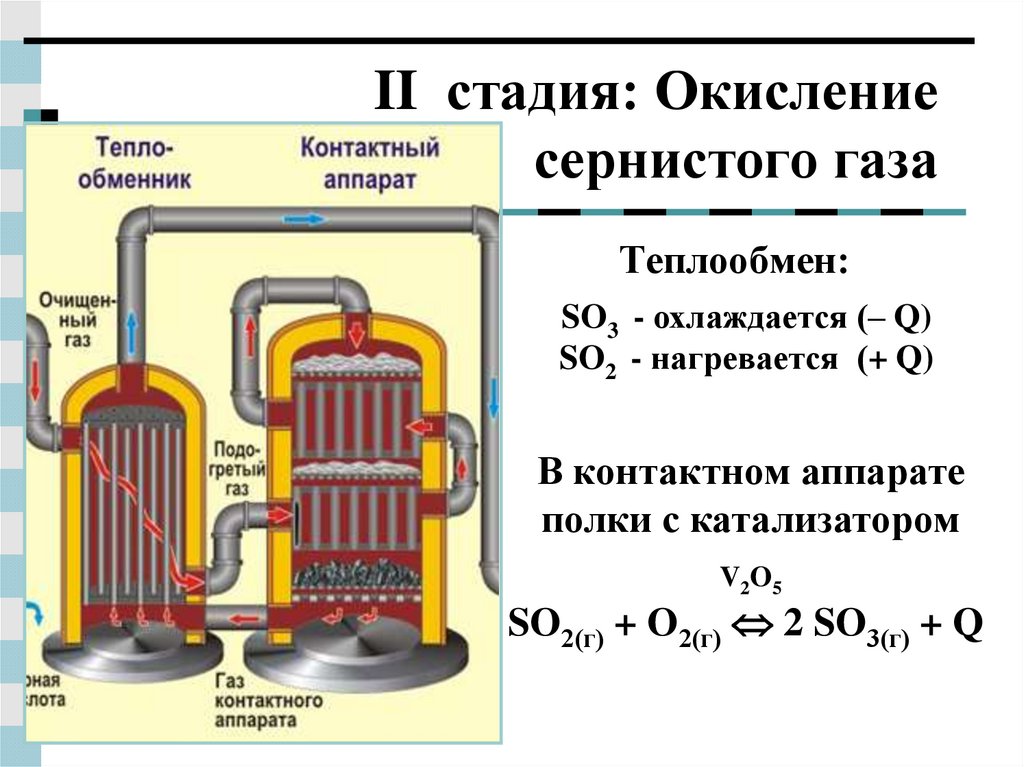
Эти цифры относятся к 2011–2012 гг. Ожидалось, что к 2012 г. мировое производство превысит 250 млн тонн (mcgroup.com) и 260 млн тонн к 2018 г. (marketsandmarkets.com) с прогнозируемой тенденцией к росту как минимум до 2023 г. (transparencymarketresearch.com).
Производство серной кислоты
Процесс производства серной кислоты состоит из четырех стадий:
a) извлечение серы
b) преобразование серы в диоксид серы
c) преобразование диоксида серы в триоксид серы
d) преобразование триоксида серы в серную кислоту
(a) Извлечение серы
Пожалуй, самый важный источник серы – это ее извлечение из природного газа и нефти. Они содержат соединения серы, как органические, так и сероводород, которые необходимо удалить перед использованием в качестве топлива или химического сырья.
Другим важным источником серы является двуокись серы при рафинировании металлов. Многие металлические руды встречаются в виде сульфидов и обжигаются с образованием оксида и диоксида серы, например, при производстве свинца:
Другие металлы, произведенные из сульфидных руд, включают медь, никель и цинк.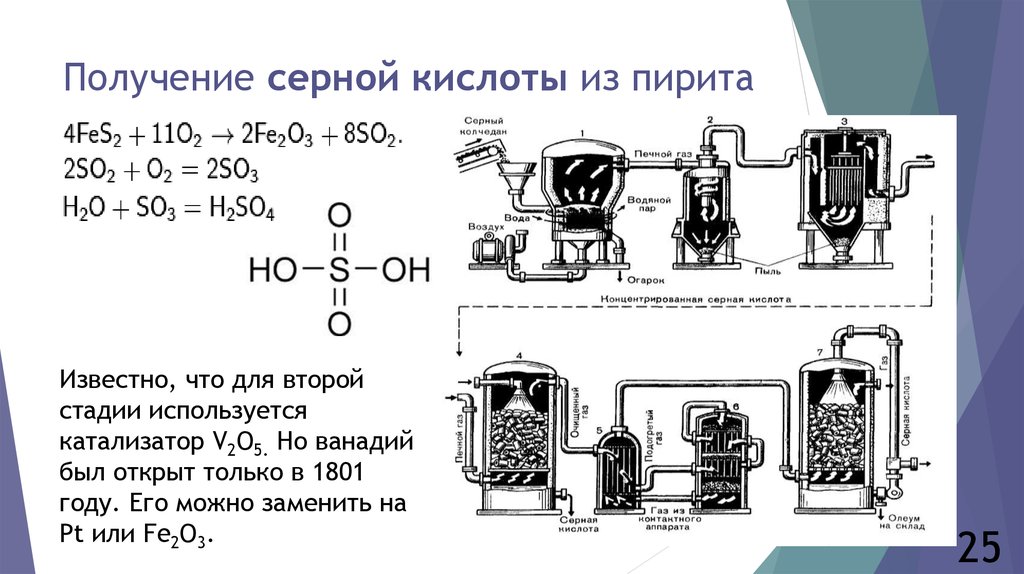
Во всем мире около 35% серы получают в виде двуокиси серы при обжиге сульфидной руды, и это число увеличивается, поскольку предприятия, которые традиционно выбрасывали двуокись серы в атмосферу, извлекают ее в виде серной кислоты. В частности, Китай производит большую часть своей серной кислоты из пирита, руды сульфида железа.
Серную кислоту также получают из сульфата аммония, побочного продукта при производстве поли(метил-2-метилпропеноата), а также извлекают из «отработанной» (т.е. использованной) серной кислоты.
(b) Конверсия серы в диоксид серы
Если сера является исходным сырьем, ее сначала необходимо преобразовать в диоксид серы. Расплавленная сера распыляется в печь и сжигается в струе сухого воздуха при температуре около 1300 К. Сера горит характерным голубым пламенем:
Поскольку используется избыток воздуха, выходящий газ содержит около 10-12% диоксида серы и 10% кислорода по объему. Газы очень горячие и поэтому проходят через теплообменники (котлы-утилизаторы).
Газы охлаждаются примерно до 700 К, а вода в окружающих трубах котла превращается в пар. При производстве одной тонны серной кислоты также производится одна тонна пара высокого давления.
(c) Конверсия диоксида серы в триоксид серы (Контактный процесс)
Типичная установка содержит один цилиндрический сосуд, который действует как реактор с неподвижным слоем с четырьмя отдельными слоями катализатора, известный как конвертер, нагретый до 700 K, через которые проходят диоксид серы и воздух:
Катализатор, оксид ванадия(V) на кремнеземе, обычно находится в форме небольших гранул, к которым в качестве промотора добавлен сульфат цезия (рис. 2). Функция промотора состоит в том, чтобы понизить температуру плавления оксида ванадия(V), чтобы он плавился при 700 K.
| В центре снимка виден газоподводящий канал. С любезного разрешения Haldor Topsøe. |
Рис. |
(d) Конверсия триоксида серы в серную кислоту
Триоксид серы, образовавшийся в третьем слое (и небольшое количество из четвертого слоя), теперь преобразуется в
серную кислоту.
Триоксид серы реагирует с водой, и реакция может быть выражена как:
Однако сама вода не может использоваться для абсорбции, так как происходит значительное повышение температуры и образуется сернокислотный туман, с которым трудно справиться. Вместо этого используется серная кислота с концентрацией около 98%. Эту концентрацию поддерживают добавлением воды и удалением кислоты при этой концентрации.
Вместо этого используется серная кислота с концентрацией около 98%. Эту концентрацию поддерживают добавлением воды и удалением кислоты при этой концентрации.
Для поддержания температуры около 400 К тепло отводится теплообменниками, рис. 4.
Рисунок 4. Линейная схема теплообменника, используемого при производстве триоксида серы.
Неабсорбированные газы содержат около 95 % азота, 5 % кислорода и следы диоксида серы. Поток газа фильтруется для удаления любых следов тумана серной кислоты и возвращается в атмосферу через высокую дымовую трубу.
Дата последнего изменения: 9 октября 2016 г.
Химическая промышленность | Обзор, важность и история
Dow Chemical Company
См. все средства массовой информации
- Связанные темы:
- Юнироял Холдингс, Инк.
Etablissements Poulenc Frères
блок операции
единичный процесс
Акзо НВ
Просмотреть все сопутствующие материалы →
химическая промышленность комплекс процессов, операций и организаций, осуществляющих производство химических веществ и их производных.
Хотя химическую промышленность можно описать просто как отрасль, которая использует химию и производит химикаты, это определение не совсем удовлетворительно, поскольку оно оставляет открытым вопрос о том, что такое химическое вещество. Определения, принятые для статистических экономических целей, варьируются от страны к стране. Кроме того, Стандартная международная торговая классификация, опубликованная Организацией Объединенных Наций, включает взрывчатые вещества и пиротехнические изделия в раздел химических веществ. Но в эту классификацию не входят искусственные волокна, хотя подготовка сырья для таких волокон так же химична, как и любая отрасль производства.
Сложные характеристики химической промышленности
Масштабы химической промышленности частично определяются обычаями, а не логикой. Нефтяную промышленность обычно считают отдельной от химической промышленности, поскольку на заре нефтяной промышленности в 19 веке сырая нефть подвергалась простой перегонке.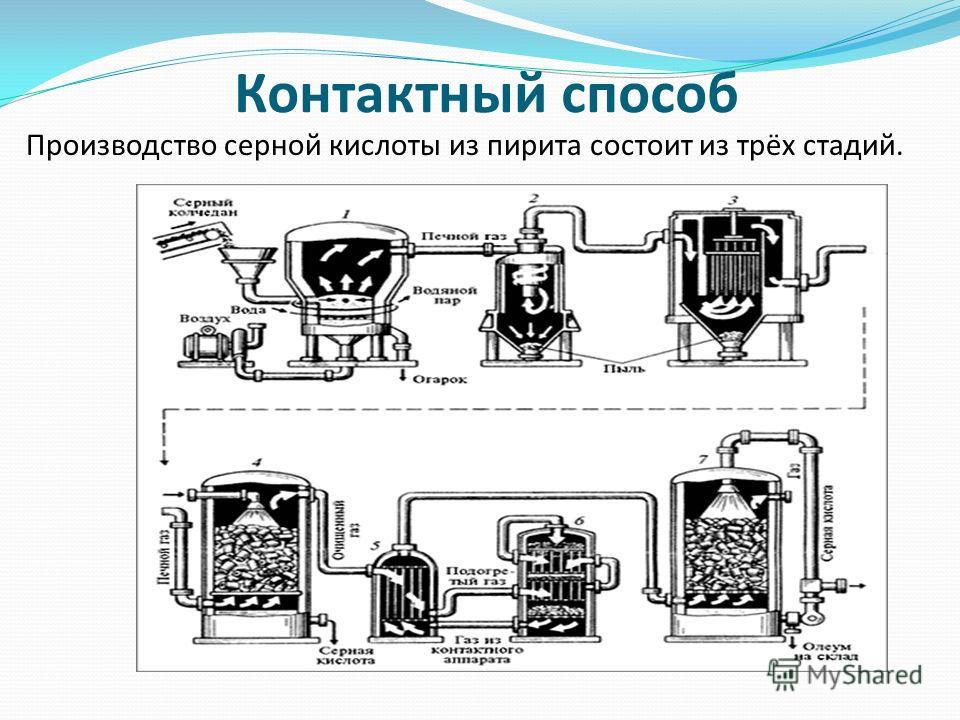 Однако современные нефтяные промышленные процессы вызывают химические изменения, и некоторые продукты современного нефтеперерабатывающего комплекса являются химическими веществами по любому определению. Термин «нефтехимия» используется для описания этих химических операций, но, поскольку они часто выполняются на том же заводе, что и первичная перегонка, трудно провести различие между нефтяной и химической промышленностью.
Однако современные нефтяные промышленные процессы вызывают химические изменения, и некоторые продукты современного нефтеперерабатывающего комплекса являются химическими веществами по любому определению. Термин «нефтехимия» используется для описания этих химических операций, но, поскольку они часто выполняются на том же заводе, что и первичная перегонка, трудно провести различие между нефтяной и химической промышленностью.
Металлы в некотором смысле являются химическими веществами, поскольку они производятся химическим путем, руды иногда требуют химического обогащения перед очисткой; процесс очистки также включает химические реакции. Такие металлы, как сталь, свинец, медь и цинк, производятся в достаточно чистом виде, а затем перерабатываются в полезные формы. Тем не менее, сталелитейная промышленность, например, не считается частью химической промышленности. В современной металлургии такие металлы, как титан, тантал и вольфрам, производятся с помощью процессов, требующих большого химического мастерства, однако они по-прежнему классифицируются как первичные металлы.
Таким образом, границы химической промышленности несколько размыты. Его основным сырьем являются ископаемое топливо (уголь, природный газ и нефть), воздух, вода, соль, известняк, сера или их эквивалент, а также некоторые специализированные виды сырья для специальных продуктов, такие как фосфаты и минеральный плавиковый шпат. Химическая промышленность превращает это сырье в первичные, вторичные и третичные продукты, причем различие основано на удаленности продукта от потребителя, причем первичный является наиболее удаленным. Продукты чаще всего являются конечными продуктами только самой химической промышленности; Главной характеристикой химической промышленности является то, что ее продукция почти всегда требует дальнейшей обработки, прежде чем попадет к конечному потребителю.
Таким образом, как это ни парадоксально, химическая промышленность сама себе лучший клиент. Средний химический продукт проходит от фабрики к фабрике несколько раз, прежде чем он попадает из химической промышленности на рынок.
Оформите подписку Britannica Premium и получите доступ к эксклюзивному контенту.
Подпишитесь сейчас
Существует множество путей к одному и тому же продукту и множество применений одного и того же продукта. Например, чаще всего этиленгликоль используется в качестве автомобильного антифриза, но он также используется в качестве гидравлической тормозной жидкости. Дальнейшая обработка приводит к получению многих производных, которые используются в качестве добавок в текстильной, фармацевтической и косметической промышленности; в качестве эмульгаторов при применении инсектицидов и фунгицидов; и как деэмульгаторы для нефти. Фундаментальные химические вещества, такие как хлор или серная кислота, используются столь многими способами, что не поддаются исчерпывающему списку.
Из-за конкуренции в химической промышленности и среди химикатов химическая промышленность тратит большие средства на исследования, особенно в высокоразвитых странах. Процент дохода, потраченного на исследования, варьируется от одной отрасли к другой; компании, специализирующиеся на крупносерийных продуктах, которые широко используются в течение многих лет, тратят меньше, тогда как конкуренцию в более новых областях можно встретить только за счет интенсивных исследований.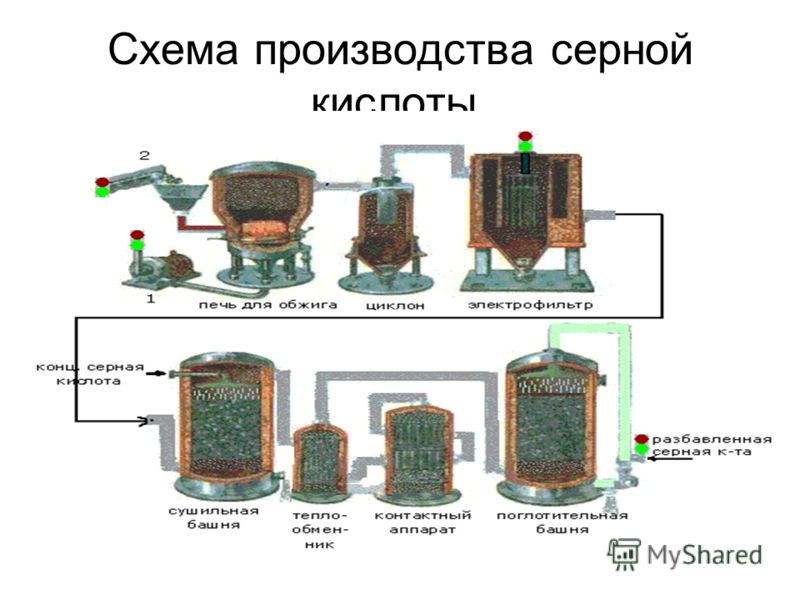
Экономические аспекты
В большинстве областей Соединенные Штаты являются крупнейшим производителем химикатов. Германия, Великобритания, Франция, Италия и некоторые другие европейские страны также являются крупными производителями, как и Советский Союз. Япония в 1960-х годах приобрела известность как очень крупный производитель в определенных областях. Инвестиции в химическую промышленность в процентах от общих инвестиций в данной стране могут составлять от 5 до 15% для менее развитых стран; для промышленно развитых стран она составляет в среднем около 6—8%. Для некоторых развивающихся стран этот процент может сильно колебаться; например, установка одного крупного завода по производству удобрений может заметно изменить процентное соотношение в конкретной стране.
В начале 20-го века существовало заметное различие между экономикой, основанной на угле как ископаемом топливе, и экономикой, основанной на нефти. Уголь был почти единственным источником ароматических углеводородов. Две силы, однако, работали вместе, чтобы изменить эту ситуацию. Во-первых, ароматические углеводороды теперь можно получать и из нефти, да и вообще все углеводородное сырье теперь почти взаимозаменяемо; во-вторых, современная транспортная техника позволяет в очень больших объемах перевозить по морю не только нефть, сырую или в различных стадиях очистки, но и природный газ, охлажденный и сжиженный до жидкого состояния.
Две силы, однако, работали вместе, чтобы изменить эту ситуацию. Во-первых, ароматические углеводороды теперь можно получать и из нефти, да и вообще все углеводородное сырье теперь почти взаимозаменяемо; во-вторых, современная транспортная техника позволяет в очень больших объемах перевозить по морю не только нефть, сырую или в различных стадиях очистки, но и природный газ, охлажденный и сжиженный до жидкого состояния.
Статистические данные химической промышленности в целом могут вводить в заблуждение из-за практики объединения таких продуктов, как недорогая серная кислота и дорогие красители или волокна; в некоторые подборки включены косметика и туалетные принадлежности, стоимость которых за фунт может быть искусственно завышена. Статистика химической промышленности разных стран может иметь разную базу расчета; действительно, база может время от времени меняться в одной и той же стране. Дополнительным источником путаницы является то, что в некоторых случаях производство указывается не в тоннах самого продукта, а в тоннах содержания важного компонента.
Для простоты различные разделы химической промышленности, такие как тяжелая неорганическая и органическая химия и различные семейства конечных продуктов, будут описаны по очереди и отдельно, хотя следует иметь в виду, что они постоянно взаимодействуют. Первый раздел, который следует обсудить, — это тяжелые неорганические химикаты, начиная с исторического начала химической промышленности с процесса Леблана. Однако термины «тяжелая химическая промышленность» и «легкая химическая промышленность» не являются полностью исключительными, поскольку многие операции находятся где-то между этими двумя классами. Однако эти два класса в своих крайностях коррелируют с другими различиями. Например, внешний вид двух видов растений характерно различен. Крупный химический завод характеризуется большими частями оборудования необычных форм и размеров, стоящими неподвижно и независимо друг от друга. Видны длинные ряды дистилляционных колонн, но, поскольку перерабатываемый материал обычно находится в трубах или сосудах, здесь не происходит никакой заметной деятельности.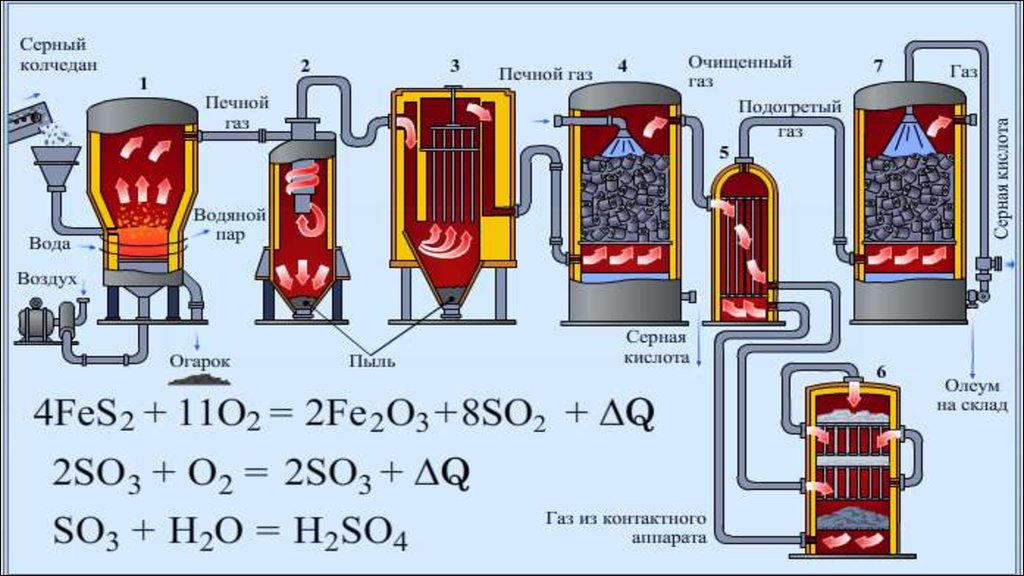
 Снизу (принцип противотока) пропускают воздух, обогащённый кислородом, для более полного обжига пирита. Температура в печи для обжига достигает 800оС
Снизу (принцип противотока) пропускают воздух, обогащённый кислородом, для более полного обжига пирита. Температура в печи для обжига достигает 800оС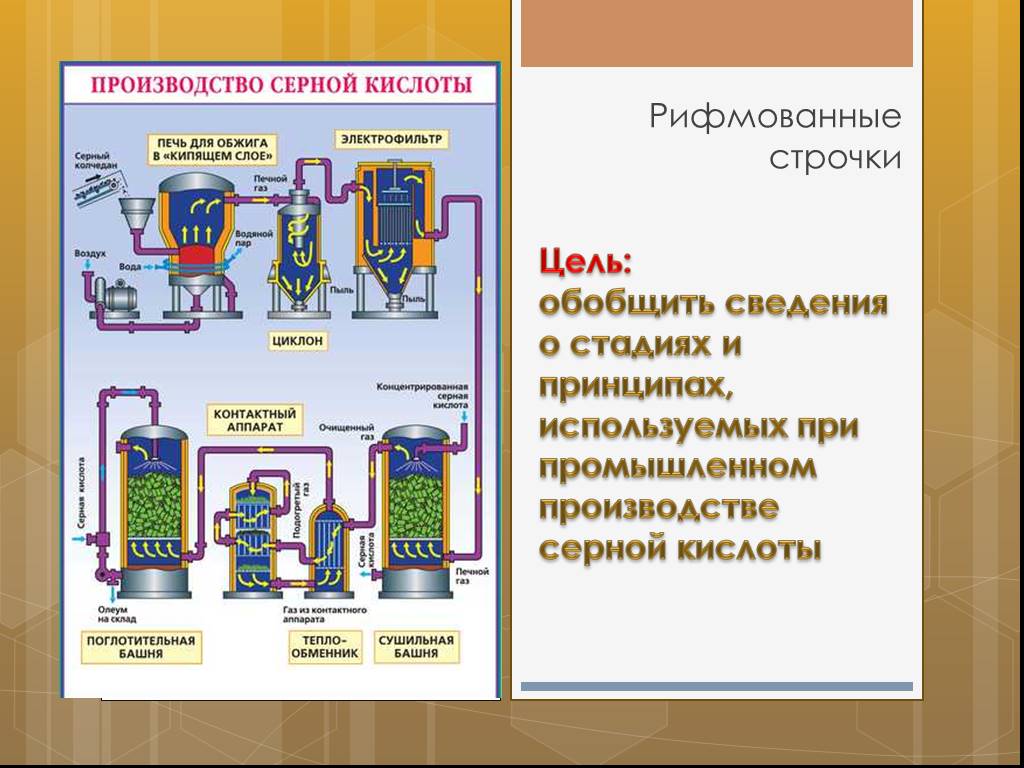 Для смещения равновесия вправо процесс проводят при повышенном давлении.
Для смещения равновесия вправо процесс проводят при повышенном давлении. Затем олеумом заполняют цистерны, формируют железнодорожные составы и отправляют потребителю.
Затем олеумом заполняют цистерны, формируют железнодорожные составы и отправляют потребителю. 3. Блок-схема процесса обращения. Как показано выше, это экзотермическая реакция, поэтому для удовлетворительного выхода триоксида серы (требуется конверсия выше 99,5%) используется настолько низкая температура, насколько это экономически возможно. Таким образом, от газа, выходящего из каждого слоя, отводится тепло с помощью теплообменников. Полученный триоксид серы удаляют между третьим и четвертым слоями и направляют на следующую стадию превращения триоксида серы в серную кислоту.
3. Блок-схема процесса обращения. Как показано выше, это экзотермическая реакция, поэтому для удовлетворительного выхода триоксида серы (требуется конверсия выше 99,5%) используется настолько низкая температура, насколько это экономически возможно. Таким образом, от газа, выходящего из каждого слоя, отводится тепло с помощью теплообменников. Полученный триоксид серы удаляют между третьим и четвертым слоями и направляют на следующую стадию превращения триоксида серы в серную кислоту.